Si l'on considère les noyaux présents dans la nature, on constate que les noyaux légers possèdent un nombres de neutrons à peu près égal au nombre de protons.
Exemple :
Le carbone 12 contient 6 protons et 6 neutrons ;
l'oxygène 16 contient 8 protons et 8 neutrons.
Pour les noyaux lourds, on constate que le nombre de neutrons devient très supérieur au nombre de protons.
Exemple :
Le plomb 208 contient 126 neutrons pour 82 protons !
On voit ainsi que lorsque la taille du noyau augmente, la proportion entre neutrons et protons augmente elle aussi. Ce phénomène permet d'augmenter la force attractive nucléaire (qui s'exerce entre tous types de nucléons - protons ou neutrons) par rapport à la force de répulsion électrostatique (qui s'exerce seulement entre protons).
En effet lorsque la taille du noyau augmente, plus précisément lorsque le numéro atomique Z et le nombre de masse A augmentent, ces forces n'évoluent pas de la même manière :
la force de répulsion électrostatique augmente en
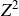 ;
;
alors que la force attractive nucléaire augmente plus lentement (augmente proportionnellement à A, approximativement).
Il faut donc ajouter plus de neutrons, lorsque le numéro atomique augmente, pour assurer la cohésion du noyau.




