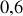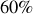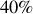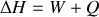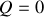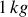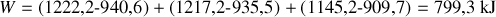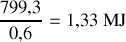Énoncé
Pour liquéfier du gaz naturel, on comprime à une pression de
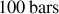 du méthane initialement à la pression de
du méthane initialement à la pression de
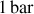 et à la température de
et à la température de
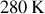 , puis on le refroidit jusqu'à
, puis on le refroidit jusqu'à
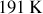 (on suppose ici que l'on dispose d'un cycle de réfrigération permettant de le faire). La compression est supposée isentropique, mais le rapport de compression très élevé nécessite le recours à plusieurs compresseurs (
(on suppose ici que l'on dispose d'un cycle de réfrigération permettant de le faire). La compression est supposée isentropique, mais le rapport de compression très élevé nécessite le recours à plusieurs compresseurs (
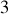 dans cet exemple) avec refroidissement intermédiaire à
dans cet exemple) avec refroidissement intermédiaire à
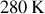 . Les pressions intermédiaires sont égales à
. Les pressions intermédiaires sont égales à
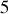 et
et
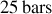 .
.
Le gaz refroidi à
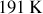 est détendu isenthalpiquement (détente de Joule-Thompson) de
est détendu isenthalpiquement (détente de Joule-Thompson) de
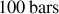 à
à
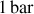 , et ses phases liquide et gazeuse à la température de
, et ses phases liquide et gazeuse à la température de
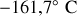 sont séparées. Ces transformations subies par le gaz sont illustrées sur la figure suivante :
sont séparées. Ces transformations subies par le gaz sont illustrées sur la figure suivante :
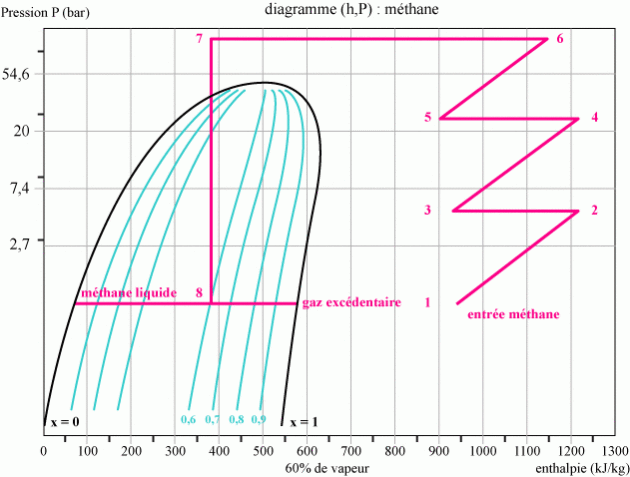
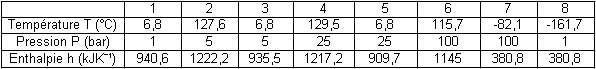
Les valeurs des enthalpies et pressions des différents points sont données dans le tableau ci-dessous.
Déterminer à partir de la figure le titre en vapeur de méthane du mélange obtenu.
Déterminer le travail de compression nécessaire pour l'obtention d'un kilogramme de méthane liquide.
Données :
Les transformations subies par le gaz et les points intermédiaires sont illustrés sur la figure 1. Les valeurs des pressions, températures et enthalpies aux différents points sont les suivants :