La variance v est le nombre de variables intensives que l'expérimentateur peut fixer séparément. Pour un corps pur unique , v=3-\phi où \phi est le nombre de phases en présence. Par exemple, pour \phi=1 on peut fixer indépendamment P et T. De même, \phi=2\Rightarrowv=1 : à température donnée, il n'existe qu'une pression sous laquelle l'équilibre entre deux phases d'un corps pur peut être réalisé, et réciproquement. Enfin, lorsque les trois phases sont en présence (point triple, v=0), toutes les variables intensives ont une valeur fixée ; ce n'est pas le cas pour les variables extensives puisque la quantité de matière n'est pas imposée : on peut décider d'amener un, deux ou dix litres du corps au point triple...
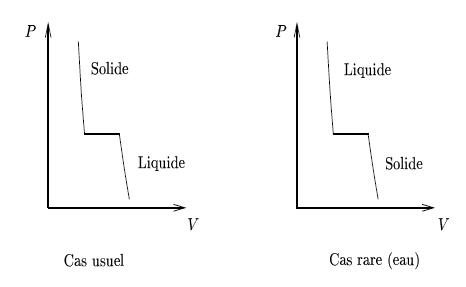
En général, lorsqu'on comprime un liquide de façon isotherme, sa pression augmente jusqu'à atteindre la pression de solidification où peuvent coexister liquide et solide.
Si l'on continue de comprimer, la pression reste constante jusqu'à ce que la dernière goutte de liquide ait disparu (on a en effet v=1). Ensuite, la pression augmente de nouveau puisque tout le liquide s'est solidifié (v=2). Ce comportement est général. Toutefois, pour quelques liquides rares dont l'eau, on peut obtenir le liquide en comprimant le solide. La figure 1 résume ces résultats dans une représentation (P,V) (un tel diagramme est appelé diagramme de CLAPEYRON).