Nous rappellerons tout d'abord la notation symbolique des éléments chimiques.
Soit un élément chimique X. On note Z, appelé numéro atomique, le nombre d'électrons de cet élément, qui lui confère ses propriétés chimiques. Chaque électron porte la charge
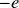 (avec e la charge élémentaire :
(avec e la charge élémentaire :
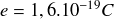 ). Le nuage électronique porte donc une charge totale
). Le nuage électronique porte donc une charge totale
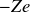 .
.
Le numéro atomique correspond également au nombre de protons contenus dans le noyau. Chaque proton porte la charge
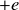 , de sorte que la charge totale du noyau est
, de sorte que la charge totale du noyau est
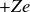 . L'atome est donc ainsi électriquement neutre.
. L'atome est donc ainsi électriquement neutre.
 Informations
InformationsSouvenons-nous que la valeur de Z définit l'élément chimique, symbolisé par une ou deux lettres (ici ce symbole est représenté par la lettre X). Par exemple l'élément carbone est caractérisé par une valeur de Z égale à 6, l'élément azote par
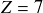 , l'élément oxygène par
, l'élément oxygène par
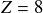 ...
...
Continuons maintenant notre description du noyau. En plus de la valeur de Z, les nucléides sont caractérisés par leur nombre de masse A. Le nombre de masse correspond au nombre total de nucléons (Z protons et N neutrons) :
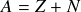 . Les neutrons sont, comme leur nom l'indique, électriquement neutres.
. Les neutrons sont, comme leur nom l'indique, électriquement neutres.
Neutrons et protons ont approximativement la même taille et la même masse. Ils font partie d'une même grande famille appelée nucléons.
Rappelons que la masse molaire d'un nucléide est en première approximation donnée par le nombre de masse (par exemple la masse molaire de l'hydrogène 1 est approximativement égale à 1 g/mol).




