Question 1
Du premier principe de conservation de l'énergie se déduisent les égalités :
 et
et
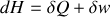 ,
,
soit
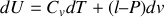 et
et
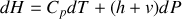 .
.
Question 2
L'équation d'état d'un gaz parfait est
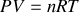 .
.
Un gaz parfait est un gaz qui obéit aux deux lois de Joule :
son énergie interne ne dépend que de la température :
 ;
;son enthalpie ne dépend que de la température :
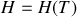 .
.
Question 3
En raison des lois de Joule, les écritures différentielles de l'énergie interne et de l'enthalpie sont nécessairement du type :
1/
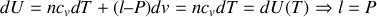
2/
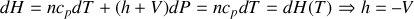
Par conséquent,
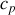 et
et
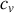 ne peuvent dépendre que d'un seul paramètre d'état, la température.
ne peuvent dépendre que d'un seul paramètre d'état, la température.
Question 4
En raison de la définition de l'entropie,
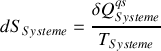 .
.
Par suite pour le gaz parfait,
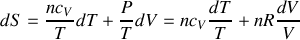
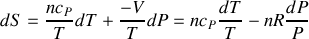
Question 5
Par intégration, il vient aisément
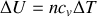 et
et
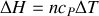 , où
, où
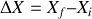 .
.
L'intégration de dS est également aisée dans la mesure où chaque dérivée partielle ne dépend que de sa variable de dérivation. Il vient les deux expressions équivalentes :
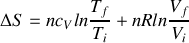
et

Question 6
En utilisant la loi de Mayer
 et le coefficient de Laplace
et le coefficient de Laplace
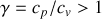 , les capacités thermiques peuvent être exprimées sous la forme :
, les capacités thermiques peuvent être exprimées sous la forme :
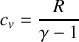 ;
;




