Héraclites, philosophe grec qui a vécu de circa – 544 à circa – 483, a maintenu que tout est dans un état de flux et que rien n'échappe au changement, posant que c'est impossible de marcher dans la même rivière (entre la décision pour le faire et de le faire la rivière change son état). En revanche Parménide, philosophe grec présocratique qui a vécu de la fin du
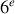 siècle au début du
siècle au début du
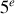 siècle, a posé que tout est ce qu'il est, donc il ne peut pas devenir ce que il n'est pas, par conséquence le changement est impossible pour toute substance.
siècle, a posé que tout est ce qu'il est, donc il ne peut pas devenir ce que il n'est pas, par conséquence le changement est impossible pour toute substance.
C'est à Démocrite, un autre philosophe grec de – 460 à – 370, que revient une hypothèse réconciliant ces deux points de vue opposés, en raison de sa conviction en un univers constitué d'atomes et de vide. Le mot atome vient du grec et signifie indivisible. Selon lui les atomes sont de petits grains de matière qui forment l'univers qui nous entoure et qui nous constitue. Entre ces atomes se trouve le vide. Ces idées préparent le terrain pour dire que les atomes sont invariables mais que leurs arrangements changent régulièrement.
Il faut attendre le début du 19e siècle pour entendre parler de nouveau d' atomes .
John Dalton est nommé professeur de philosophie naturelle au New College de Manchester en 1793.

Ses premiers travaux scientifiques suscitent peu d'intérêt mais plus tard en 1803, il propose pour la première fois une théorie selon laquelle la matière est composée d'atomes de masses différentes. Cette théorie, qui est sa plus importante contribution à la science, expose que :
Les éléments sont faits de particules minuscules appelées atomes qui ne peuvent pas être créés, ou divisés en plus petites particules, ni détruits dans les processus chimique.
Tous les atomes d'un élément donné sont identiques.
Les atomes d'un élément donné sont différents de ceux de tout autre élément.
Les atomes d'un élément peuvent combiner avec les atomes d'autres éléments pour former des composés chimiques ; un composé a toujours les mêmes nombres relatifs de ces composantes atomiques.
Une réaction chimique change simplement la manière dont les atomes sont arrangés et groupés ensemble.
En 1808 Dalton publie son livre, Un nouveau système de philosophie chimique, où il dresse la liste des masses atomiques d'un certain nombre d'éléments, rapportés à la masse de l'Hydrogène. Même si certaines valeurs ne sont pas entièrement correctes, ses masses forment la base de la table périodique moderne des éléments, un repère indispensable pour la physique nucléaire.
Dans ce livre, Dalton présente des symboles sphériques pour décrire les atomes des éléments.
Quelques années plus tard William Prout, un médecin et biochimiste à Londres, propose comme hypothèse en 1815 que l'Hydrogène est le protyle, une substance primitive hypothétique sur laquelle les éléments chimiques sont supposés être formés.




