Rutherford avait envisagé le proton en 1914 lorsque certaines de ces expériences l'ont conduit à suggérer que le noyau de l'Hydrogène était le porteur de charge positive et masse dans la structure de tous les atomes plus lourds. Toujours passionné par la structure nucléaire, il prépare en 1919 une expérience pour bombarder les noyaux d'azote au moyen de particules alpha émises par le Polonium.
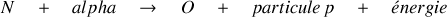
Le bombardement fait apparaître que l'Oxygène est une particule chargée
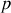 , sa charge positive (
, sa charge positive (
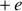 ) étant égale à la charge de l'électron, et sa masse égale à environ la masse de l'Hydrogène. Les véritables réactions nucléaires verront ainsi le jour. Par la nature de cette réaction, Rutherford concluait alors que la particule
) étant égale à la charge de l'électron, et sa masse égale à environ la masse de l'Hydrogène. Les véritables réactions nucléaires verront ainsi le jour. Par la nature de cette réaction, Rutherford concluait alors que la particule
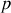 est intimement liée au noyau de l'Hydrogène. L'idée qu'il avait avancée en 1914 se trouve donc appuyée par ces résultats de 1919 même si, très prudent, il ne voulait pas s'exprimer définitivement sur le sujet.
est intimement liée au noyau de l'Hydrogène. L'idée qu'il avait avancée en 1914 se trouve donc appuyée par ces résultats de 1919 même si, très prudent, il ne voulait pas s'exprimer définitivement sur le sujet.
Remarque :
De plus, quatre fois la masse de cette particule
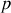 fait environ la masse de la particule alpha et deux fois sa charge fait la charge de l'alpha. Dès lors Rutherford a soupçonné qu'il y a deux types de particules élémentaires au noyau de l'Hélium : une neutre et l'autre porteur de charge, mais à masses égale. Plus tard ces deux particules seront appelées le proton et le neutron. Il faut en effet deux protons et deux neutrons pour constituer la particule alpha.
fait environ la masse de la particule alpha et deux fois sa charge fait la charge de l'alpha. Dès lors Rutherford a soupçonné qu'il y a deux types de particules élémentaires au noyau de l'Hélium : une neutre et l'autre porteur de charge, mais à masses égale. Plus tard ces deux particules seront appelées le proton et le neutron. Il faut en effet deux protons et deux neutrons pour constituer la particule alpha.
La particule
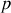 prend son nom de proton lors d'un évènement bien identifié
, à la réunion de l'Association Britannique pour l'Avancement de Science le mercredi 25 août, 1920, à Cardiff. Lors de la Séance A, Rutherford présenta une communication intitulée La Construction d'Atomes résumant ces idées sur le noyau de l'Hydrogène et sur ses résultats à l'égard de la particule
prend son nom de proton lors d'un évènement bien identifié
, à la réunion de l'Association Britannique pour l'Avancement de Science le mercredi 25 août, 1920, à Cardiff. Lors de la Séance A, Rutherford présenta une communication intitulée La Construction d'Atomes résumant ces idées sur le noyau de l'Hydrogène et sur ses résultats à l'égard de la particule
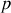 , considérée comme le noyau de l'Hydrogène. Lors de la discussion qui a suivi, un autre physicien, Oliver Lodge, lui demande de donner un nom à cette particule pour éviter la confusion possible entre atome et noyau de l'Hydrogène. Rutherford réplique immédiatement en citant deux noms : proton et prouton. Les deux sont en effet appropriés. Proton porte la racine grecque pour « première ». Prouton fait l'écho du nom de Dr W. Prout, le médecin londonien qui avait proposé en 1815 l'hypothèse que l'Hydrogène soit considéré comme la substance primitive sur laquelle les éléments chimiques sont formés ; si cette hypothèse n'était pas confirmée elle continuait à être citée. C'est le nom proton qui a duré dans le temps.
, considérée comme le noyau de l'Hydrogène. Lors de la discussion qui a suivi, un autre physicien, Oliver Lodge, lui demande de donner un nom à cette particule pour éviter la confusion possible entre atome et noyau de l'Hydrogène. Rutherford réplique immédiatement en citant deux noms : proton et prouton. Les deux sont en effet appropriés. Proton porte la racine grecque pour « première ». Prouton fait l'écho du nom de Dr W. Prout, le médecin londonien qui avait proposé en 1815 l'hypothèse que l'Hydrogène soit considéré comme la substance primitive sur laquelle les éléments chimiques sont formés ; si cette hypothèse n'était pas confirmée elle continuait à être citée. C'est le nom proton qui a duré dans le temps.
L'atome, l'électron et le proton sont maintenant connus. Mais il reste encore quelques mystères. En fait, ce nouveau modèle atomique va à l'encontre des lois de la physique. Comment expliquer que les électrons puissent graviter autour du noyau positif de l'atome sans jamais s'écraser dessus ? Comment se déplacent-ils autour du noyau ? Quelle est leur distribution ? Comment les protons chargés positivement surmontent-ils la force de répulsion électrique qui devrait normalement les éloigner les uns des autres et provoquer l'éclatement du noyau ? Les réponses viendront de Niels Bohr et de James Chadwick.
Remarque :
C'est grâce aux expériences d'E. Rutherford et de ses collaborateurs que les notions physiques à l'égard de l'atome et de son noyau ont commencé à être clarifiées. Ces expériences révélèrent que la matière a des charges positives réparties différemment des charges négatives au sein de l'atome. Plus précisément on commença alors à comprendre que les atomes avaient un noyau minuscule positivement chargé constitué des protons et que les électrons dans ces atomes étaient assez loin du noyau. E. Rutherford a reçu le prix Nobel de chimie en 1908 pour ses travaux sur la radioactivité.




