On néglige les interactions entre les particules, alors l'énergie totale est purement cinétique. Pour une particule confinée dans une boîte de taille ![]() par un potentiel infini le Hamiltonien vaut :
par un potentiel infini le Hamiltonien vaut :
avec P sa quantité de mouvement.
A une dimension
Posons l'équation de Schrödinger stationnaire :
avec ![]() et
et ![]() .
.
Les conditions aux limites fixes sont :
La solution de l'équation (1) s'écrit sous la forme :
La première condition aux limites
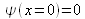 donne
donne 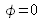
La deuxième condition aux limites
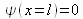 donne
donne 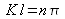
Condition de normalisation :
alors : ![]() car
car ![]() .
.
On a donc en réinjectant dans l'équation de Schrödinger :
et nous remarquons que l'énergie est quantifiée.
A trois dimensions
Le hamiltonien ![]() s'écrit sous la forme :
s'écrit sous la forme :
La fonction d 'onde ![]() peut être séparée suivant les trois directions de l'espace car l'équation est linéaire.
peut être séparée suivant les trois directions de l'espace car l'équation est linéaire.
L'énergie du système s' écrit :
L'équation ![]() donne que l'énergie du gaz parfait unidimensionnel peut se mettre, en décalant l'indice d'un cran pour partir de 0, sous la forme :
donne que l'énergie du gaz parfait unidimensionnel peut se mettre, en décalant l'indice d'un cran pour partir de 0, sous la forme :
avec :![]() .
.
La fonction de partition du gaz parfait vaut donc :
En supposant que l'énergie ![]() varie d' une façon continue (ce qui est acceptable pour les grandes énergies) alors :
varie d' une façon continue (ce qui est acceptable pour les grandes énergies) alors :
or ![]() donc par symétrie (fonction paire) :
donc par symétrie (fonction paire) : ![]()
D'autre part, on a :
avec ![]() .
.
![]() est dite longueur d'onde thermique de de Broglie. Remarquons que cette longueur est caractéristique du côté quantique du système : pour un système de grandes dimensions par rapport à elle, le système est classique. Ceci se produit pour des petites valeurs de
est dite longueur d'onde thermique de de Broglie. Remarquons que cette longueur est caractéristique du côté quantique du système : pour un système de grandes dimensions par rapport à elle, le système est classique. Ceci se produit pour des petites valeurs de ![]() , des grandes masses ou des températures élevées.
, des grandes masses ou des températures élevées.
Généralisation à 3 dimensions :
La fonction de partition vaut ![]() à partir de la forme de l'équation de Schrödinger. Remarquons par exemple pour l'argon dans les conditions normales de température et de pression que cette longueur d'onde de de Broglie est très faible devant les distances moyennes interatomiques, donc les atomes d'argon dans ces conditions peuvent être traités par la mécanique classique. Par contre, pour l'hélium, plus léger, aux basses températures, ou pour des électrons d'un solide à température ambiante, confinées dans une maille cristalline, la longueur d'onde de de Broglie est plus grande que les dimensions caractéristiques du problème, ce qui implique un traitement purement quantique.
à partir de la forme de l'équation de Schrödinger. Remarquons par exemple pour l'argon dans les conditions normales de température et de pression que cette longueur d'onde de de Broglie est très faible devant les distances moyennes interatomiques, donc les atomes d'argon dans ces conditions peuvent être traités par la mécanique classique. Par contre, pour l'hélium, plus léger, aux basses températures, ou pour des électrons d'un solide à température ambiante, confinées dans une maille cristalline, la longueur d'onde de de Broglie est plus grande que les dimensions caractéristiques du problème, ce qui implique un traitement purement quantique.
Calcul de l'énergie moyenne d 'un gaz parfait
En utilisant les formules vues précédemment :
or :
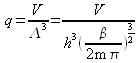
alors : ![]() .
.
En dérivant seul subsiste le terme en ![]() donc :
donc : ![]() , avec N le nombre de particules.
, avec N le nombre de particules.
Pour n moles, le nombre de particules est ![]() avec
avec ![]() .
.
la capacité calorifique vaut donc
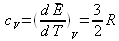 pour le gaz monoatomique ce qui correspond à un résultat connu en thermodynamique classique. C'est un premier argument pour identifier le paramètre
pour le gaz monoatomique ce qui correspond à un résultat connu en thermodynamique classique. C'est un premier argument pour identifier le paramètre 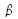 avec la température thermodynamique
avec la température thermodynamique 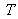 ,
,
pour le gaz diatomique nous verrons à la fin du cours que :



