L'énergie
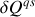 échangeable par chaleur par
échangeable par chaleur par
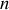 moles de gaz parfait peut aussi s'exprimer en fonction de la température
moles de gaz parfait peut aussi s'exprimer en fonction de la température
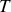 et de la pression
et de la pression
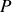 :
:
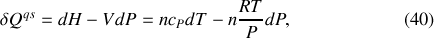
où
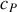 est la capacité thermique molaire à pression constante du gaz parfait. De cette équation se déduisent directement:
est la capacité thermique molaire à pression constante du gaz parfait. De cette équation se déduisent directement:
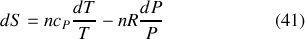
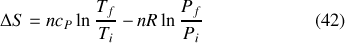
Remarque :
le rapport des températures peut ici être remplacé par le rapport des enthalpies (de préférence molaires). La capacité thermique étant assimilée à une constante, température et enthalpie sont en effet proportionnelles ;
les équations (37) et (42) sont strictement équivalentes en raison de la Loi des gaz parfaits (27) et de la Loi de Mayer pour le gaz parfait :

les équations (37) et (42) peuvent par ailleurs être appliquées à n'importe laquelle des transformations du gaz parfait, même si elles ne sont pas quasi-statiques, dès lors qu'elles le font passer d'un état d'équilibre initial à un état d'équilibre final. Il est parfaitement inutile d'en refaire le calcul pour chaque type de transformation.




